
Ученые в США разработали новую мощную систему редактирования генома, которая может предложить значительно большую точность и эффективность, чем текущий стандарт CRISPR .
В то время как CRISPR-Cas9 является революционной медицинской технологией, которая закладывает современные основы для редактирования генетического кода, включая варианты, связанные с заболеванием, уже давно существуют опасения относительно его неточности.
В частности, многие опасаются, что редактирование CRISPR-Cas9 потенциально может привести к ошибкам в виде неконтролируемых вставок и удалений в генетическом коде, называемых инделами.
Исследователи говорят, что новая система, названная ее изобретателями в Институте Широкого Массачусетского технологического института и Гарвардском университете, называется «первичное редактирование», и она может изменить игру благодаря новому белку, который обеспечивает высокоточное редактирование генетических целей.
«Главное стремление в области молекулярных наук о жизни — это способность точно вносить любые изменения в геном в любом месте», — говорит биолог из генома Дэвид Лю из Института Броуд.
«Мы не знаем о другой технологии редактирования в клетках млекопитающих, которая предлагает этот уровень универсальности и точности с таким небольшим количеством побочных продуктов».
Основой нового простого метода редактирования является фермент, называемый обратной транскриптазой. Система CRISPR также использует фермент — Cas9 — для разрезания нитей ДНК, чтобы можно было вставить альтернативный генетический код.
Прорыв 2017 года, впервые осуществленный лабораторией Лю, значительно повысил точность системы, позволив однобуквенным изменениям в парах оснований ДНК вместо замены целых участков кода сразу.
Теперь, благодаря обратной транскриптазе, которая используется вместе с Cas9 в первичном редактировании, геномное редактирование снова обновлено.
В простом редактировании направляющая РНК, называемая pegRNA, направляет модифицированную форму фермента Cas9, чтобы обрезать только одну цепь ДНК (предотвращая разрывы двух нитей, которые могут вызвать непреднамеренные нарушения).
После этого фермент обратной транскриптазы непосредственно копирует отредактированную генетическую информацию, содержащуюся в пегРНК, в целевой геномный сайт. Вы можете увидеть подробное объяснение процедуры в инфографике ниже:
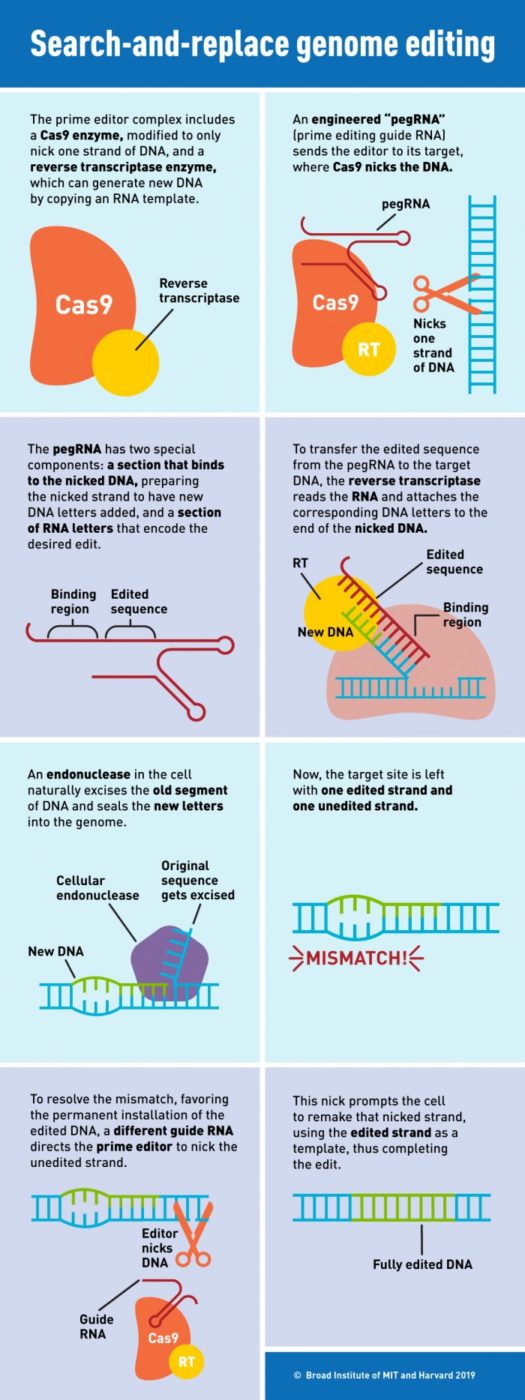
«Универсальность простого редактирования быстро стала очевидной, когда мы разработали эту технологию», — объясняет химик-биолог Эндрю Ансалоне.
Гибкость системы означает, что впервые исследователи могут эффективно менять одну «букву» ДНК на другую — среди химических веществ аденин (A), цитозин (C), гуанин (G) и тимин (T) — во всех 12 возможных способов.
Это явное улучшение того, на что способны основные усовершенствования редакторов, сделанные в 2017 году , что означает, что теперь возможны совершенно новые виды генетических изменений при заболеваниях людей по сравнению с тем, что можно было сделать раньше.
«Благодаря первичному редактированию мы теперь можем напрямую исправить мутацию серповидно-клеточной анемии обратно в нормальную последовательность и удалить четыре дополнительных основания ДНК, которые вызывают болезнь Тея Сакса, без разрезания ДНК полностью или необходимости шаблонов ДНК», — объясняет Лю.
В новой статье исследователей команда детализирует эти процедуры в лабораторных тестах, среди которых более 175 изменений в клетках человека и мыши — с результатами, которые дали меньше нежелательных побочных продуктов, и представили меньшее количество нецелевых изменений, чем подход Cas9 сам по себе создал бы.
Это знаковые вещи, но особенно учитывая быстрые темпы развития этих технологий, исследователи стремятся подчеркнуть, что мы все еще только в начале тестирования системы, чтобы выяснить, на что она способна в лабораторной среде.
«Необходимы дополнительные исследования для дальнейшего понимания и улучшения первичного редактирования в широком диапазоне типов клеток и организмов, для оценки нецелевого первичного редактирования в масштабе всего генома и для дальнейшей характеристики степени влияния основных редакторов на клетки пишут авторы в своей статье.
Тем не менее ясно, что здесь может быть огромное количество возможностей с точки зрения расширения теоретической и практической шкалы редактирования генома — расширения метода, в принципе, до 89 процентов известных патогенных генетических вариантов человека, говорят исследователи.
Коммерческие возможности также потенциально огромны. В то время как исследователи будут предоставлять другим исследователям некоммерческую лицензию для изучения этого подхода, коммерческие заявки на запатентованную систему могут быть более чем значительными для ее изобретателей.
Результаты представлены в .
